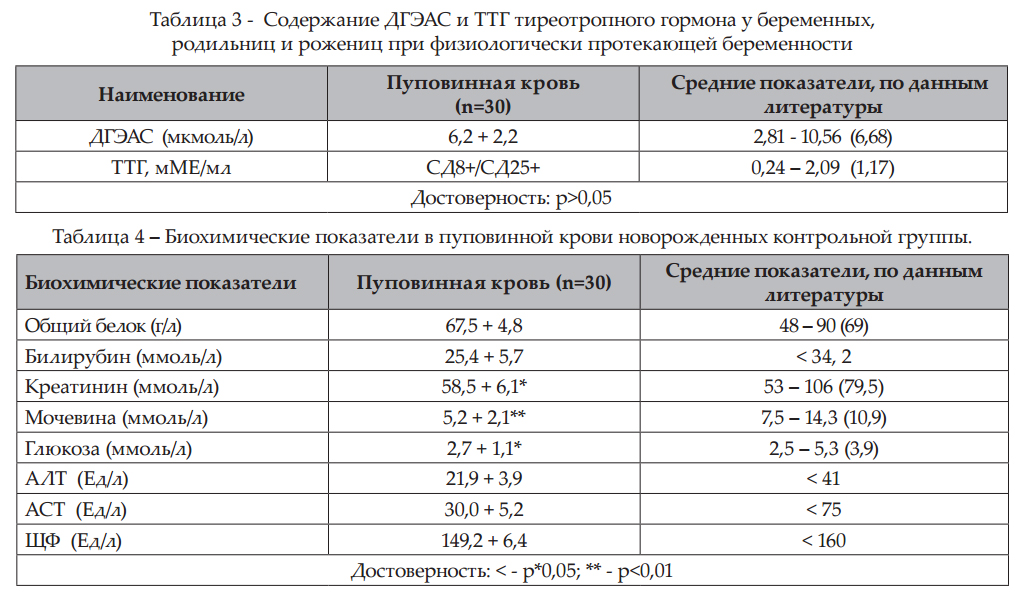
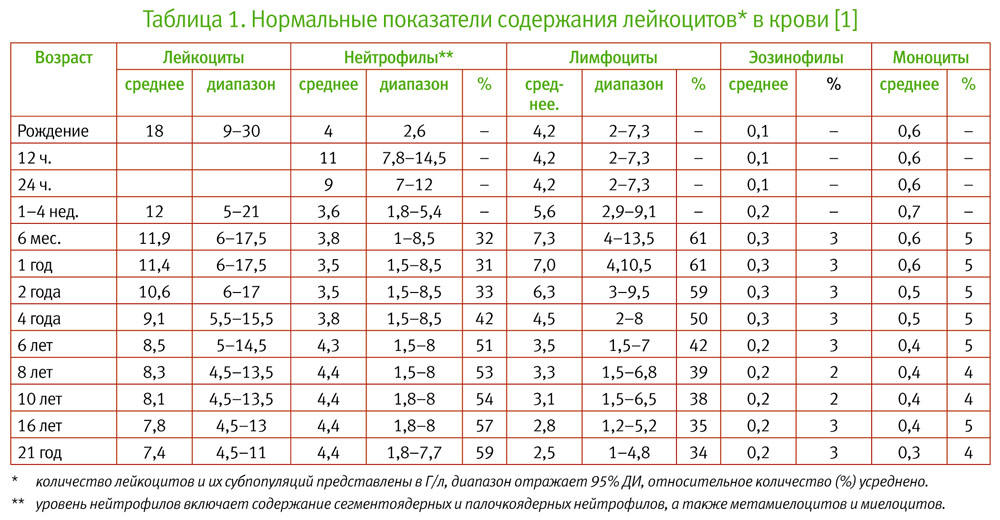
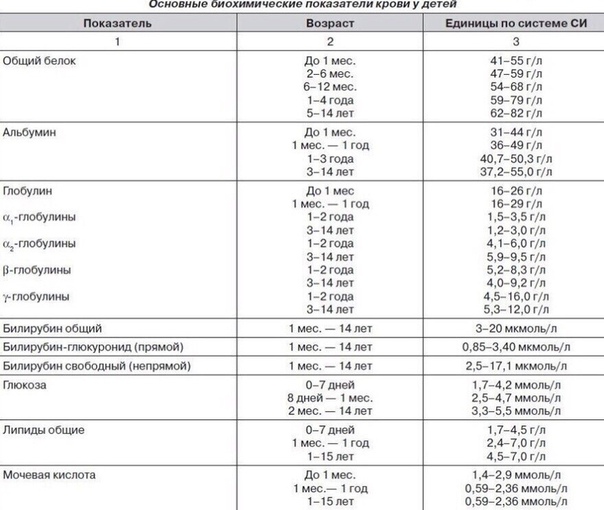
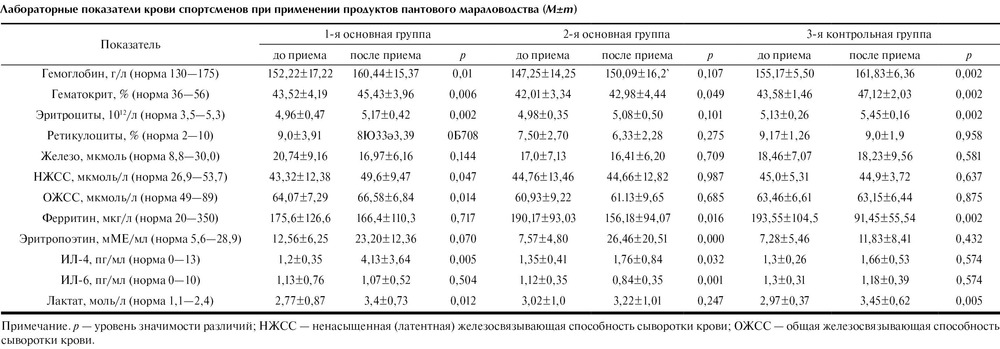
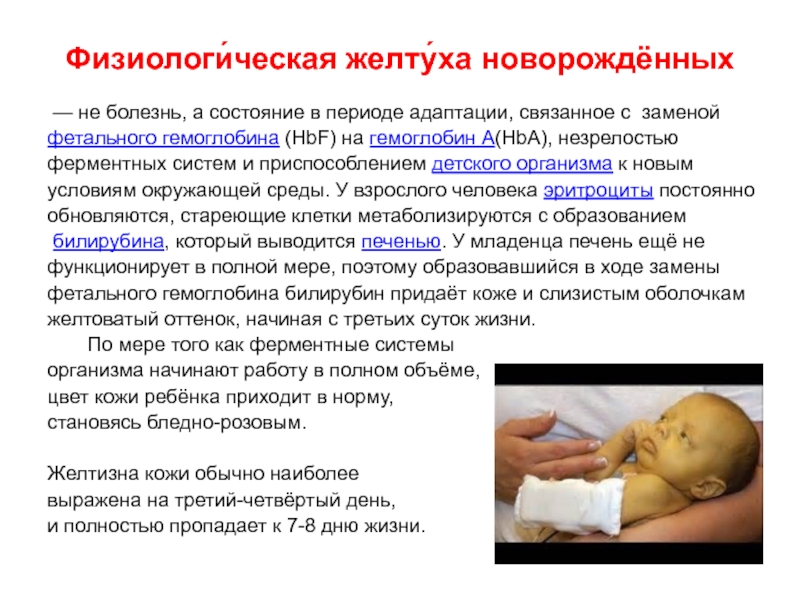
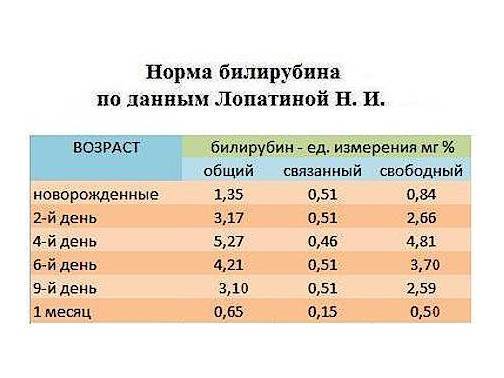
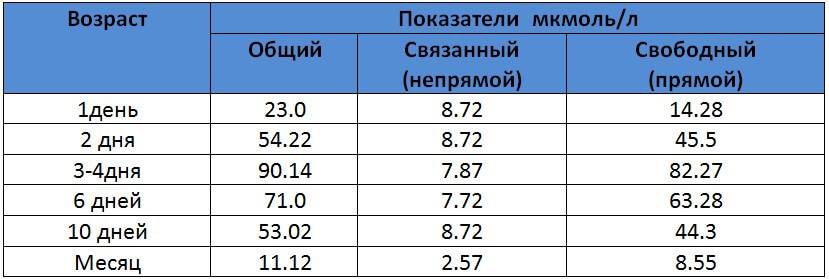
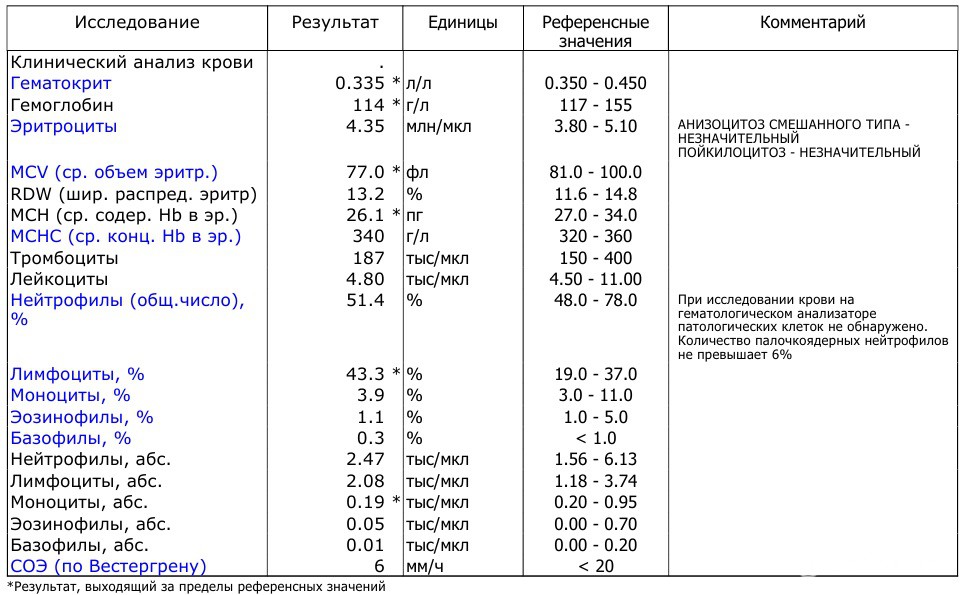
Норма ЛДГ
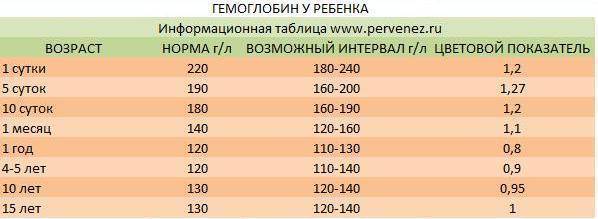
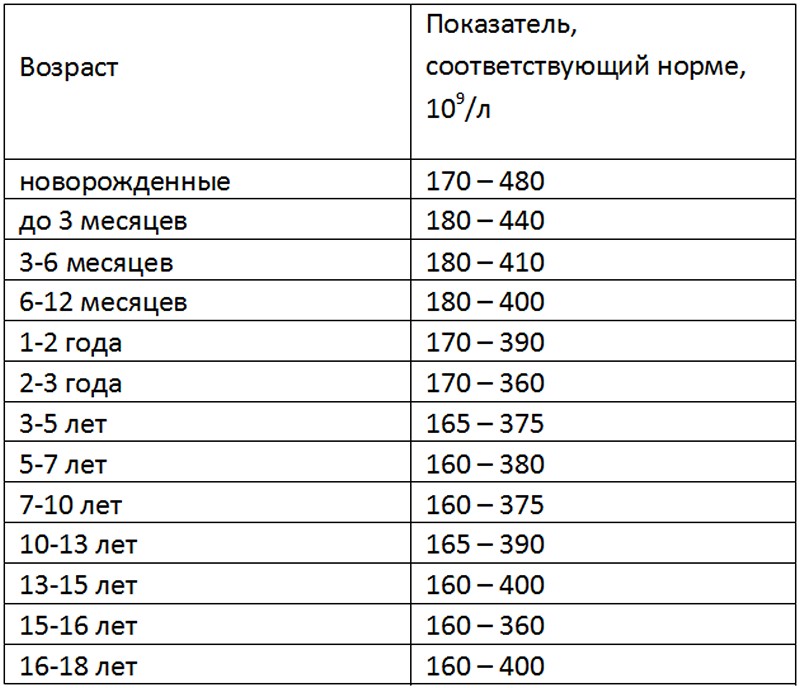
Норма ЛДГ в крови у женщин, детей и мужчин меняется в соответствии с возрастом человека. Расшифровка показателей лактатдегидрогеназы для детей определяется по таблице:
| Возраст | Показатели, норма (Ед/л) |
| до 1 года | до 450 |
| 2–3 года | до 345 |
| 4–6 лет | до 315 |
| 7–12 | до 300 |
| 13–18 | до 270 |

У людей, старше 18 лет нормальные показатели определяются в соответствии с полом. Так, для женского организма этот параметр может меняться от 13 до 220 Ед/л. У мужчин при норме значения LDG выше, чем у женщин и составляют 130 – 235 Ед/л.
Значительное снижение или увеличение единиц свидетельствует о развитии патологий. Но, следует учитывать, что несоответствие референсным показателям может возникать вследствие неправильной подготовки к биохимическому анализу: чрезмерной физической активности, приеме определенных препаратов.
Симптомы муковисцидоза
Специалисты выделяют несколько форм заболевания: кишечную, легочную и смешанную.
К основным симптомам заболевания обычно относят:
- отсутствие аппетита, крики и громкий плач у грудничков и новорожденных;
- вздутие живота;
- ощущение сухости во рту.
Симптомы муковисцидоза зависят от формы болезни. Муковисцидоз легких сильно снижает иммунитет, а поскольку слизистые пробки легко поражаются бактериями стафилококка или синегнойной палочки, люди постоянно страдают от повторяющихся бронхитов и пневмоний.
Основные признаки муковисцидоза легких1:
- частые респираторно-вирусные заболевания;
- постоянный приступообразный кашель с густой и плохо отделяемой мокротой;
- склонность к воспалению легких и бронхитам на фоне ОРВИ*;
- жесткое дыхание, появления свистящих хрипов при простудах и вирусных заболеваниях;
- появление одышки, признаков гипоксии;
- снижение веса, авитаминозы;
- изменение формы грудной клетки, которая приобретает вид лодочного киля, может становиться бочкообразной;
- ногтевые пластины, кончики пальцев приобретают вид барабанных палочек.
Кишечная форма муковисцидоза характеризуется ферментной недостаточностью, нарушением всасывания полезных веществ в кишечнике. В результате нехватки ферментов стул становится «жирным», могут активно размножаться бактерии, в результате чего накапливаются газы, что приводит к выраженному метеоризму. Стул учащается, а объем каловых масс может в несколько раз превышать возрастную норму.
У детей кишечная форма муковисцидоза протекает с повышенной вязкостью слюны и сильной жаждой. Аппетит может быть снижен из-за нарушения пищеварения, постоянных болей в животе и метеоризма. С первых дней жизни ребенок может страдать кишечной непроходимостью, которая обусловлена нехваткой фермента трипсина, отвечающего за расщепление белков. В результате в тонком кишечнике происходит накопление мекония — плотной, густой массы темно-коричневого цвета. У ребенка появляются запоры и частые срыгивания, возможно возникновение рвоты. Помимо симптомов со стороны желудочно-кишечного тракта (ЖКТ) заболевание может сказываться на общем состоянии организма, поскольку качественное питание оказывает прямое влияние на развитие ребенка. Из-за нехватки полезных веществ могут появляться слабость, ломкость костей, ухудшаться состояние кожи, ногтей, волос1.
Смешанная форма заболевания характеризуется сочетанием поражения кишечника и бронхолегочной системы. Это проявляется и в симптомах: люди со смешанной формой муковисцидоза страдают от частых вирусных заболеваний, затяжного кашля и одновременно от нарушения пищеварения, метеоризма1.
Независимо от формы болезни одним из частых симптомов муковисцидоза является соленый вкус кожи больного. Это объясняется повышенным содержанием хлоридов в поте и на протяжении долгого времени являлось ключевым признаком для постановки диагноза1.
Лечение
Чем ранее проведены диагностические мероприятия и выявлена патология, тем успешнее лечение галактоземии. Терапия зависит от тяжести состояния. Обычно она длительная и требует слаженной работы врачей и родителей.
Питание
В основе эффективного лечения лежит принцип замены молока миндальными либо соевыми смесями (это безлактозные смеси). Сегодня практически нет проблем с возможностью приобретения смесей и продуктов питания без лактозы. Ассортимент детского питания в супермаркетах и специализированных магазинах огромен. Производители указывают на упаковке состав продукции и предупреждающие надписи (содержит или не содержит смесь молочный сахар).
Прикорм рекомендуется вводить в более раннем возрасте – около 4 месяцев (для здоровых детей рекомендуемый возраст введения прикорма – это около полугода жизни ребенка).
Приблизительно с 4-месячного возраста специалисты рекомендуют начинать кормить ребенка соком. Для этого постепенно и в очень небольших количествах вводятся фруктовые и ягодные натуральные соки. Не стоит вводить сразу несколько видов фруктов! С 4,5 месяцев малыш может попробовать пюре из фруктов, в 5 месяцев – пюре из овощей, а с 5,5 месяцев – первую кашу. Каши готовятся из кукурузы, гречки, риса. Вместо молока используется овощной отвар, альтернатива отвару – каши, разведенные безлактозным молочком. В полгодика ребенку можно давать мясо: выбираются обезжиренные сорта (птица, говядина, кролик), рыбу вводят в 8 месяцев.
Постепенно следует расширять палитру вкусовых ощущений для малыша
Каждый новый продукт нужно вводить осторожно, тщательно следя за реакцией организма на новую еду. Обычно строгое ограничение лактозы соблюдается до 5 лет (после можно частично компенсировать неправильный ферментный синтез, но не всегда!)
Если степень патологии средняя или тяжелая, то диета сохраняется навсегда. Рацион не должен содержать лактозу, сахарозу, крахмал, т.е. то, что обостряет состояние. Углеводы поступают из альтернативных источников (фруктоза).
Применение лекарств
Диагностика галактоземии
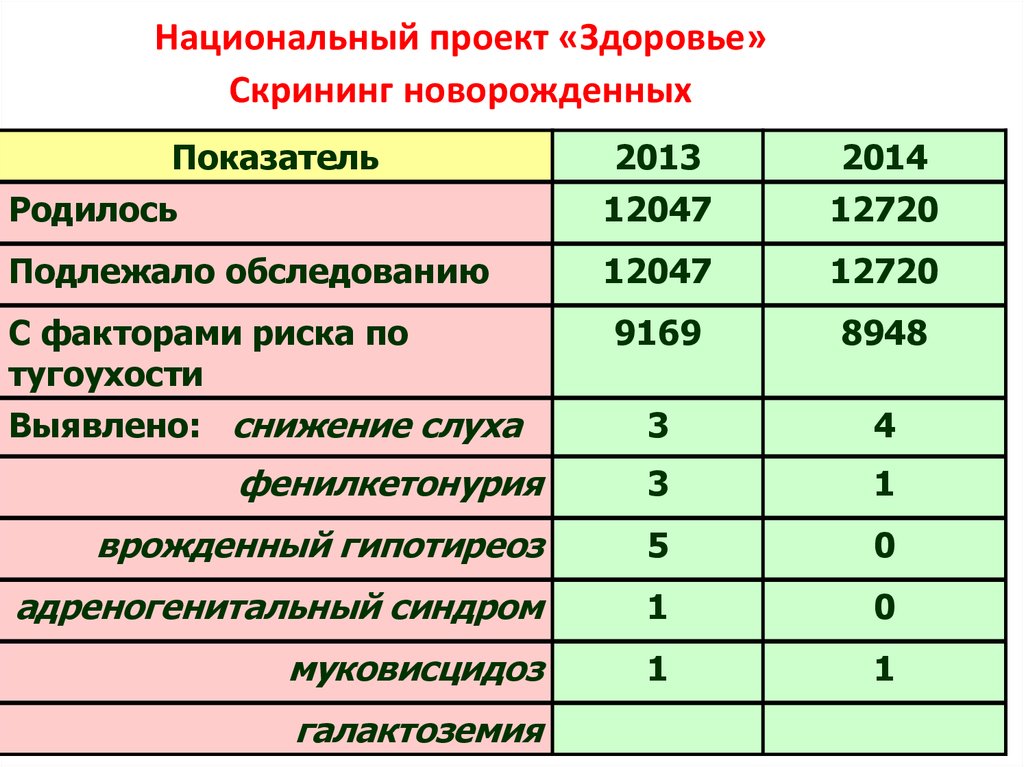
С целью снижения риска развития осложнений очень важной является как можно более ранняя диагностика галактоземии. На сегодняшний день во многих родильных домах у всех новорожденных в обязательном порядке берется анализ на галактоземию (скрининг)
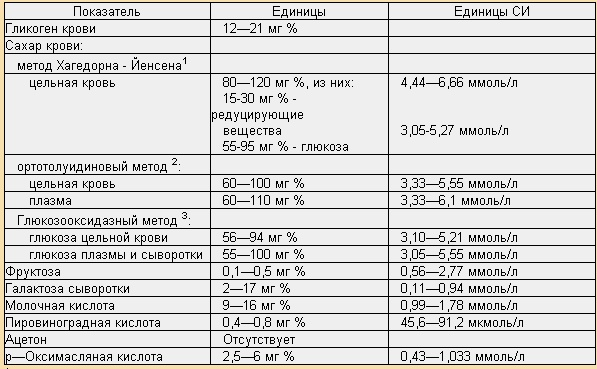
Лабораторные методы диагностики галактоземии сводятся преимущественно к обнаружению повышенного содержания галактозы в моче и крови. Помогает установить правильный диагноз проведение теста на всасывание D-ксилозы и нагрузочные пробы с галактозой и глюкозой. Несомненным подтверждением наличия галактоземии у пациента служит генетическое тестирование, благодаря которому врачи выявляют мутантный ген, отвечающий за развитие заболевания.
К неспецифическим лабораторным анализам на галактоземию относятся биохимический анализ крови и общий анализ мочи. Эти методы позволяют определить, как прогрессирует заболевание и степень поражения внутренних органов. Для этих же целей широко применяют инструментальные методы диагностики (электроэнцефалография, изучение хрусталика глаза при помощи щелевой лампы, УЗИ органов брюшной полости, пункционная биопсия печени).
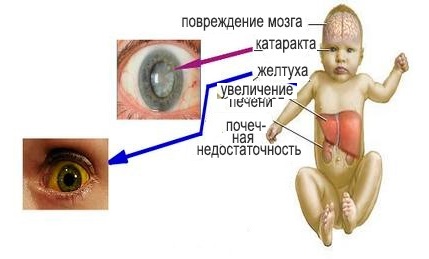
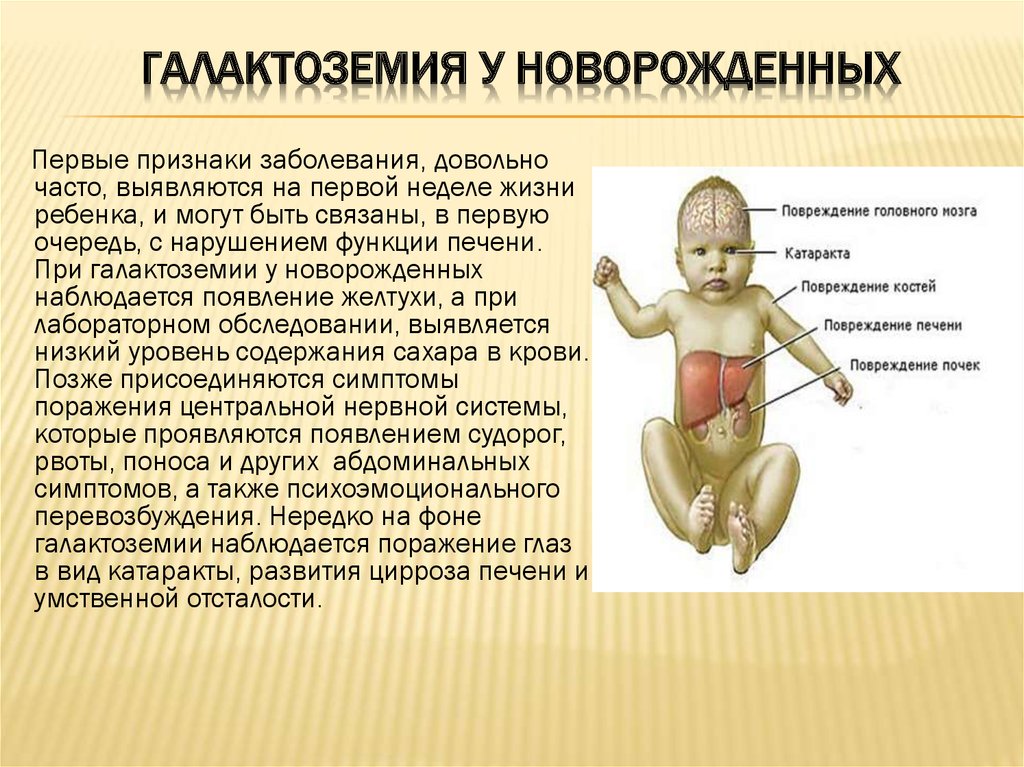
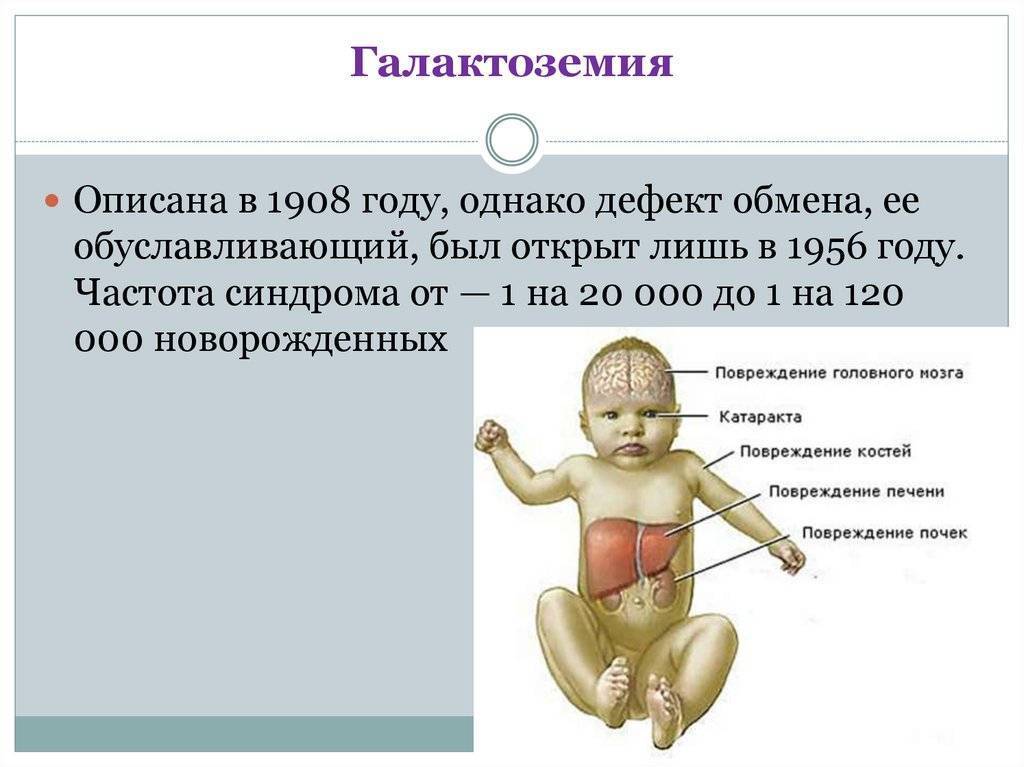
Симптомы
Наиболее важные проявления патологии – это непереносимость любого молока, в составе которого имеется лактоза, а также развитие желтухи, катаракты (сложная болезнь глаз), гепатомегалии, цирроза, истощения ввиду нарушения пищеварения.
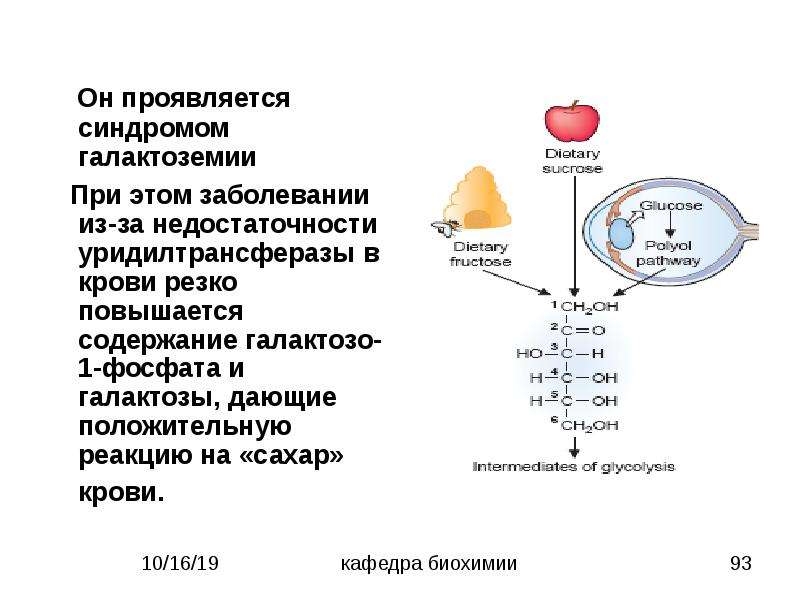
Симптомы галоктоземии у новорожденных развиваются из-за значительного повышения концентрации токсичных веществ в крови и появления реакции торможения ферментов на активность токсинов. Ферменты, участвующие в метаболизме углеводов, не могут снизить плотность галактозы (а также ее обменных продуктов), поэтому развивается гипогликемический синдром, оказывающий негативное влияние на ряд внутренних органов.
Распространенные признаки галактоземии. Виды патологии
Классический: обусловлен недостатком галактозо-1-фосфат уридилтрансферазы (это фермент, который участвует в преобразовании галактозы в глюкозу). При недостаточном количестве этого фермента происходит повышение галактозы в крови и уменьшение глюкозы. Печень неполноценно участвует в обмене D-галактозы (составной части молока). Симптомы галактоземии при классическом типе – это большая масса тела новорожденного ребенка. Дополнительно в ближайшее время после родов, после того, как малыш выпьет молоко, у него возникает жидкий стул и/или сильная рвота. Стремительно развивается гипотрофия (дефицит массы тела, истощение), появляется пожелтение склер глаз, кожи. Печень увеличивается, развиваются признаки катаракты (она вызвана образованием галактита в глазном хрусталике по причине расстройства электролитного баланса и повышения галактозы). Часто развивается гемолитическая форма анемии (распад эритроцитов).
Недостаточность галактокиназы проявляется только одним признаком – развитием катаракты. Чтобы понять, что у новорожденного ребенка развивается именно галактоземия, исследуются биологические жидкости. Анализ крови покажет увеличение галактозы и галактитола. Моча насыщается восстанавливающими веществами. Симптомы катаракты развиваются очень быстро, и галактоземия прогрессирует при отсутствии лечения. При своевременной терапии патологические процессы в глазах обратимы.
Недостаточность эпимеразы мало изучена. Патология этого типа почти не имеет физических проявлений, отмечается биохимическими сдвигами, выявляемыми случайно (обнаруживается повышение моносахарида). Данный тип болезни не требует экстренной терапии.
Галактоземия у новорожденных выдает симптоматику в первые 3–10 дней после рождения. В организм ребенка поступает молоко, а вместе с ним вещества, которые не могут перевариться и усвоиться. Постепенно токсины накапливаются. Метаболизм фермента протекает в печени, после чего он поступает в кровяное русло.
Что такое ППЦНС?
Само словосочетание перинатальный период говорит о том, что перинатальное поражение ЦНС развивается у еще не родившегося или только появившегося на свет ребенка.Перинатальное поражение центральной нервной системы (ППЦНС) — это не один, а несколько диагнозов, которые подразумевают нарушение функций работы в головном мозге новорожденного ребенка и могут привести к стойким неврологическим последствиям в более старшем возрасте (например, ДЦП, ЗПРР).
Весь перинатальный период условно делится на три этапа:
– с 28 недели и до момента родов длится антенательный период;
– сам процесс родов называется интранатальным периодом;
– неонатальный период это промежуток времени с момента рождения до 7 дня жизни включительно.
В современной медицине нет точного названия заболевания при поражении ЦНС плода, есть только сборное, его называют ППЦНС или же перинатальная энцефалопатия. Перинатальное поражение ЦНС у новорожденных, проявляется нарушениями в работе двигательного аппарата, нарушением речи и психики.
С развитием медицины, перестали данный диагноз употреблять для детей старше одного месяца. По истечении месяца врач должен поставить точный диагноз ребенку. Именно в этот период невролог с точностью определяет, насколько сильно повреждена нервная система. Назначает лечение и следит за тем, чтобы оно было подобрано правильно.
Каковы причины и факторы риска ППЦНС?
Причины, по которым может развиться перинатальное поражение центральной нервной системы достаточно разнообразны, среди самых популярных:
– соматическое заболевание матери, которое сопровождается хронической интоксикацией;
– наличие острых инфекционных заболеваний или хронических очагов инфекции, в то время когда будущая мать вынашивала ребенка;
– в случае, если у женщины нарушен процесс питания, или же она не созрела для беременности и родов;
– нарушение маточно-плачцентарного кровотока во время беременности;
– изменения в обмене веществ также влечет за собой расстройство нервной системы у будущего ребенка (повышение уровня биллирубина, неонатальная желтуха);
– в случае сильного токсикоза, как на ранней стадии, так и на поздней, или появление иных проблем с вынашиванием ребенка;
– окружающая среда выступает немаловажным фактором в развитии заболевания;
– появление патологии во время родов — это может быть слабая родовая деятельность, ускоренные роды;
– если ребенок рождается недоношенным, то и его организм не развит полностью, поэтому на данном фоне может появиться нарушение в работе ЦНС;
– наибольшему риску развития поражений ЦНС подвержены малыши, у которых присутствует наследственный фактор.
Все остальные причины возникновения ППЦНС ситуативные и в большей степени предугадать их появление просто нельзя.
Выделяют несколько путей развития перинатального поражения ЦНС у новорожденных детей в зависимости от причины и последующей симптоматики, анализ которых позволяет поставить первоначальный диагноз:
– Если четко зафиксирован недостаток кислорода, во время нахождения малыша внутри организма матери (гипоксия), то диагностируют гипоксическое поражение ЦНС.
– Во время родов у младенца может быть повреждена тканевая структура (это может быть как головной мозг, так и спинной). В этом случае, уже идет речь о травматическом поражении ЦНС, в результате чего появляются изменения в работе головного мозга.
– В случае нарушения обмена веществ могут появиться метаболические и токсико-метаболические поражения. Это может быть связано с употреблением во время беременности алкоголя, лекарственных препаратов, никотина.
– Изменения в ЦНС при наличии инфекционных заболеваний перинатального периода.
Фибриноген у детей
В детском возрасте (до 18 лет) норма фибриногена в крови слегка отличается от «взрослых» показателей. Вне зависимости от пола, у детей нормой фибриногена считается значение 1,25—4 г/л. Исключением из этой группы становятся новорожденные дети, у которых значение фибриногена колеблется в пределах 1,25—3 г/л.
Показатель фибриногена у детей отличается от «взрослых» значений потому, что в детском возрасте система гомеостаза еще формируется, как и многие другие системы организма. С течением времени норма фибриногена у ребенка приближается к «взрослым» цифрам.
Как видно, ответ на вопрос о значении фибриногена для организма человека далеко не однозначен, как ожидалось. Уровень фибриногена в крови человека зависит от множества факторов, а повышение или снижение его концентрации нередко становится важнейшим маркером воспалительного процесса. Лабораторный симптом повышения или снижения белка — яркий маркер, который позволит врачу заподозрить некоторые патологии у пациента. Доктора активно используют анализ на фибриноген для оценки системы гомеостаза пациентов, назначения схемы лечения и контроля динамики терапии пациентов.
Описание
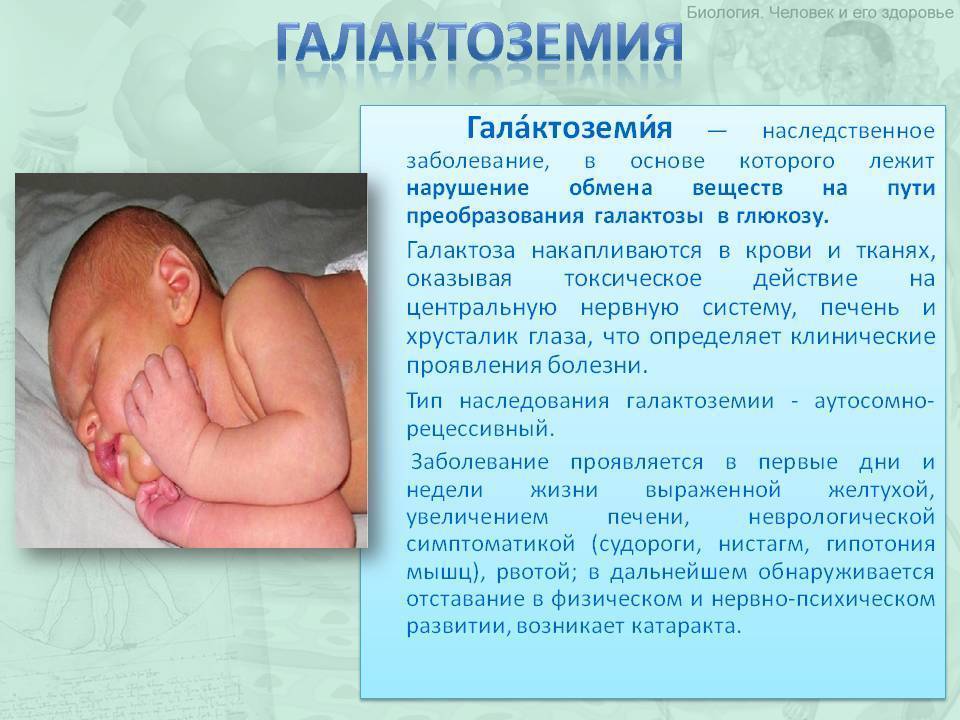
Галактоземия относится к ряду врожденных наследственных патологий. Встречается это заболевание в медицинской практике достаточно редко.
Связывают развитие патологии с недостаточной активностью необходимых для нормального процесса обмена веществ ферментов, «перерабатывающих» галактозы.
Впервые описали клинику галактоземии в 1908 г. (хотя некоторые относят к данному факту только 1917 г.). К сожалению, но подопытным ребенком стал тот, который страдал истощением, увеличением селезенки и печени. Утверждается, что вся эта симптоматика исчезла после того, как малышу отменили молочное питание.
Когда назначается исследование?
Определение фибриногена в крови врачи назначают в таких клинических ситуациях:
- если у пациента было массивное кровотечение или эпизод тромбоза;
- для оценки других показателей свертывания крови, которые определяются при исследовании крови на коагулограмму;
- при подозрении на прогрессирование заболевания печени, потому что фибриноген синтезируется именно в этом органе;
- при подозрении на наличие у пациента гемофилии или других патологий свертывающей системы крови;
- в предоперационном периоде для уверенности в том, что можно проводить хирургическое вмешательство;
- в восстановительном периоде после операции для оценки интенсивности заживления ран, активности воспаления;
- при патологии в работе сердечно—сосудистой системы;
- при наличии активного процесса воспаления, развивающегося по неизвестной причине.
Фибриноген норма у женщин особенно важна для определения во время беременности. Беременная женщина должна сдавать анализ на фибриноген один раз в триместр для того, чтобы доктор мог вовремя предупредить развитие осложнений.
Лечение ЗПРР при хромосомных заболеваниях.
Основой лечения является уникальная методика патогенетической терапии речевых расстройств при хромосомной патологии — биофизическая активация нейромоторных структур, основу которого составляет щадящая стимуляция проводников нервной системы микротоками с использованием нейрофизиологического прибора. Метод лечения базируется как на активации самих речевых центров, так и на восстановлении нарушенных связей между центрами и полушариями головного мозга. Помимо этого, восстанавливаются разрозненные связи речевых центров с другими областями мозга, участвующими в реализации речевой функции. В процессе лечения формируется физиологичное, последовательное взаимодействие всех зон мозга, связанных с речепродукцией. В результате появляется речь.
Проведение биофизической активации сочетается с дополнительными методиками лечения, такими как — лимфомежклеточная терапия, которая применяется для регулирования интегративной деятельности и восполнения дефицита энергетической системы мозга и позволяющая применять малые дозы церебропротекторов, которые вводятся эндолимфатически и попадают в ткани головного мозга, минуя гематоэнцефалический барьер.
В качестве другого способа использования препаратов с нейротрофическим и антиоксидантным действием применяется методика эндоназального электрофореза кортексина, что позволяет вводить лекарственные препараты непосредственно в ткани головного мозга.
Исследования последних десятилетий выявили, что у большинства детей с речевыми и поведенческими проблемами в различной степени нарушены функции мозжечка и базальных ганглиев. Именно функционирование мозжечка определяет успешность ребенка в обучении. С этой целью применяется уникальная разработка Центра авиакосмической медицины — подошвенный имитатор опорной нагрузки «Корвит», применяемый для нейрофизиологической регуляции стато-кинетической функции ЦНС. В основе терапевтического воздействия аппарата «Корвит» лежит процесс активации опорной афферентации, отвечающей за нормализацию процессов возбуждения и торможения в центральной нервной системе, что приводит к уменьшению спастичности мышц, развитию и закреплению функциональных связей в головном мозге, способствующих восстановлению координации движений, и, опосредованно, улучшению речи и мышления.
Также для успешного лечения различных форм ЗПРР специалистами применяется одно из достижений современной науки — метод аудиовокальной терапии RUSTOMATIS. Прибор использует звукозаписи высокочастотных и низкочастотных компонентов. При чередовании такой музыки путем напряжения и расслабления у ребенка тренируется аппарат среднего уха – молоточек и стремечко, с помощью чего расширяется диапазон восприятия внешних факторов, увеличивается концентрация внимания, в мозг поступает новая информация и, как следствие исчезают многие нарушения и расстройства.
Обязательным звеном в лечебном комплексе у детей с наличием речевых расстройств является занятия с клиническим психологом, а также логопедическая коррекция, которая включает диагностику степени нарушений, ежедневные занятия, направленные на улучшение речевой функции и логопедический массаж для коррекции различных видов дизартрии и дисфагии.
На фоне сочетания проведения биофизической активации со вспомогательными методиками лечения наблюдаются положительные изменения, которые могут быть видны уже через несколько процедур, но максимальный эффект развивается через полтора-три месяца после курса. Как правило, для закрепления полученных результатов и дальнейшего развития двигательных и когнитивных навыков специалистами центра рекомендуется повторный курс лечения через 5-6 месяцев.
Методика определения
Стандартизированная методика оценки нормы МНО была принята профильной международной организацией в 1983 году.
Во время исследования забор крови у пациента проводят из любой периферической вены, как и при других методах диагностики — общем анализе крови, биохимическом анализе крове и прочих исследованиях. В пробирке происходит смешивание крови со специальным реагентом, который выполняет функцию консерванта (цитрата). Цитрат в пробирке необходим для того, чтобы связать ионы кальция и не дать крови быстро свернуться. Затем происходит отделение плазмы от клеток, в ней находящихся. На следующем этапе проводят исследование исключительно чистой сыворотки.
В лабораторных условиях к исследуемой плазме добавляют кальций для того, чтобы нейтрализовать консервант. Затем специалист оценивает время, которое понадобилось для того, чтобы произошла реакция свертывания. Таким образом, полученное время — это показатель протромбинового времени. Затем, на основании ПТВ, специалист проводит расчет МНО.
МНО = (ПТВ пациента/ПТВ контрольной плазмы)*МИЧ, где:
*ПТВ контрольной плазмы — это стандартный показатель ПТВ капиллярной крови человека, имеющего нормальное количество факторов свертывания.
Исключительно благодаря анализу МНО можно без погрешности сравнить данные, говорящие о работе свертывающей системы крови человека, полученные в разных лабораториях и в разные промежутки времени. Норма МНО — это классический стандарт, который используется в лабораториях всех стран мира, оценивается одинаково всеми врачами.
Какие еще бывают типы
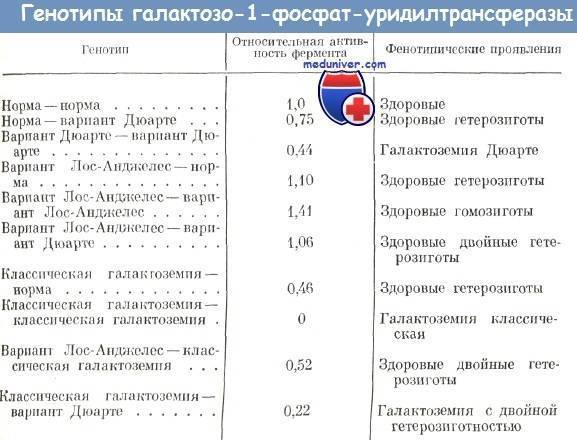
- Другой вариант классической галактоземии (тип I) — форма Дуарте. Это более легкая форма, активность фермента ГАЛТ при таком варианте может достигать 25%, а иногда и выше. Тяжелых жизнеугрожающих проявлений у новорожденных обычно не наблюдается, но могут быть желтуха, увеличение печени и задержка физического развития.
- Тип II. Характеризуется мутацией в гене GALK1, кодирующем фермент галактокиназу 1. Симптомы выражены не так сильно, как при классической галактоземии. Часто единственное проявление заболевания — развитие катаракты.
- Тип III. Характеризуется мутацией в гене GALE, кодирующем фермент эпимеразу. Может быть в легкой и тяжелой форме. Легкая форма считается доброкачественной, она связана с дефицитом фермента только в циркулирующих клетках крови. Клинических симптомов в таком случае может и не быть. При тяжелой форме фермента не хватает во всех тканях организма. Симптоматика схожа с классической галактоземией.
- Тип IV. Характеризуется мутацией в гене GALM, кодирующем фермент галактозмутаротазу. Из 8 пострадавших детей, о которых известно, ни у одного не было желудочно-кишечных симптомов или тяжелого нарушения функции печени. У двоих наблюдалась двусторонняя катаракта. Все имели нормальный рост и развитие.
Что делать при повышенном/ пониженном уровне гормона кортизола
Даже при наличии перечисленных выше симптомов нельзя самостоятельно ставить диагнозы. Не сможет этого сделать и врач, собрав только анамнез пациента. Чтобы подтвердить догадки, необходимо сдать анализ. В зависимости от случая специалист может назначить один или несколько видов лабораторных исследований:
- крови;
- слюны;
- мочи.
Каждый их них результативен в конкретных ситуациях. Для диагностики и дифференциации диагноза может быть предложено взять несколько образцов в течение одного дня. Это позволит оценить динамику и определить проблемы. Также для контроля показателей врач может назначить повторные исследования через несколько дней, чтобы исключить негативное воздействие внешних факторов, мешающих определить реальный уровень гормонов. Для подтверждения некоторых диагнозов могут одновременно браться анализ крови и мочи, слюны. Особенно часто все методы исследования назначаются при подозрении на синдром Иценко-Кушинга.
Когда назначается анализ?
Случаев, когда врач может посчитать такое исследование необходимым, очень много. Например, у женщин это нужно:
- для контроля протекания беременности;
- при нарушениях менструального цикла, изменения обильности;
- при раннем половом созревании;
- появлении волосяного покрова по мужскому типу.
В общих случаях назначается анализ при:
- патологиях костной системы и суставов, раннем остеопрозе;
- гиперпигментации и депигментации на коже;
- кожных покровах бронзового оттенка;
- красные или фиолетовые растяжки на коже в районе живота, бедер, груди;
- в течение долгого времени человек испытывает слабость в мышцах;
- угревая сыпь вне пубертатного и подросткового возраста;
- снижение веса без видимой причины;
- повышенное АД в раннем возрасте без наличия явных сердечно-сосудистых заболеваний.
Врач при сборе анамнеза оценивает жалобы пациента, которые помогут определить план диагностики и дифференциации основного диагноза. При наличии ярко выраженных симптомов колебаний гормона кортизола могут быть назначены соответствующие исследования с целью подтвердить или исключить диагноз.
Разновидности лактазной недостаточности
В зависимости от причин, бывает первичная и вторичная лактазная недостаточность.
Первичная лактазная недостаточность связана с врожденным дефицитом фермента лактазы. Этот вид заболевания встречается крайне редко.
Лечением первичной лактазной недостаточности будет являться снижение количества лактозы в пище (лактоза содержится в молоке, а также во всех блюдах и продуктах, в состав которых входит молоко), вплоть до полного исключения.
Вторичная лактазная недостаточность связана с повреждением клеток кишечника и, как следствие, уменьшением выработки лактазы. Именно такой тип заболевания чаще всего диагностируют у малышей педиатры. Хорошие новости для родителей – такая лактазная недостаточность, как правило, носит временный характер и проходит при восстановлении слизистой кишечника. «А что же это за причины, которые приводят к повреждению клеток кишечника?», – спросите Вы. Это может быть аллергия на белок коровьего молока, наличие у ребенка паразитов (лямблии, глисты), кишечные инфекции (ротавирусная, энтеровирусная), воспалительные заболевания кишечника.
В таком случае особое внимание должно быть уделено лечению основного заболевания, из-за которого и развилась вторичная лактазная недостаточность. Также необходимо снизить количество лактозы в питании малыша, но только на тот период, пока слизистая оболочка его тонкой кишки полностью не восстановится.. Не рекомендуется полностью исключать лактозу из питания грудного ребенка, ведь она важна для развития головного мозга и зрения, а также для поддержания кишечной микрофлоры крохи
Давайте подробнее рассмотрим, как снизить количество лактозы на разных типах вскармливания.
Не рекомендуется полностью исключать лактозу из питания грудного ребенка, ведь она важна для развития головного мозга и зрения, а также для поддержания кишечной микрофлоры крохи. Давайте подробнее рассмотрим, как снизить количество лактозы на разных типах вскармливания.
Если Ваш малыш находится на естественном вскармливании, врач может рекомендовать использование препаратов лактазы, которые смешиваются со сцеженным грудным молоком и расщепляют лактозу, не оказывая влияния на его остальные свойства.
В случае искусственного вскармливания следует заменить смесь на специальную низколактозную. Безлактозные продукты назначаются при тяжелых формах лактазной недостаточности, когда использование низколактозных смесей неэффективно.
Важно подобрать смесь, содержащую максимально возможное количество лактозы, которое не будет вызывать появления у малыша симптомов лактазной недостаточности. Так, содержание лактозы в смеси Similac Низколактозный составляет 0,2 г на 100 мл (при стандартном разведении)
Она не уступает по безопасности и переносимости современным базовым молочным смесям и обеспечивает те же темпы физического развития, что и смеси с нормальным содержанием лактозы. Отсутствие в составе пальмового масла и наличие пребиотиков способствует комфортному пищеварению малыша, а нуклеотиды помогают развить у крохи иммунитет.
Помните: лактазная недостаточность у грудничков в большинстве случаев является решаемой проблемой. Запаситесь терпением: зачастую достаточно просто скорректировать питание ребенка, и он почувствует себя лучше. Здоровья Вашему малышу!
Материал подготовлен на основании источников:
1. Мухина Ю.Г., Шумилов П.В., Дубровская М.И. и др. Современные подходы к диагностике и терапии дисахаридазной недостаточности у детей. Трудн. пациент. 2006; 9 (4): 12-16.
2. Питание здорового и больного ребенка. Пособие для врачей под ред. Тутельяна В.А., Коня И.Я., Каганова Б.С. Москва, 2013. — 264 с.
3. «Программа оптимизации вскармливания детей первого года жизни в Российской Федерации», М.: Союз педиатров России, 2019.
Подготовка к анализу
Оценка уровня фибриногена проводится при сдаче пациентом классического биохимического анализа крови или крови на коагулограмму. В этом случае в лаборатории у человека набирают венозную кровь. Для получения корректного результата перед исследованием необходимо строго соблюдать несколько правил.
За 10—12 часов до забора крови запрещено употреблять пищу, то есть, на исследование необходимо прийти натощак. За 2—3 суток до диагностики следует отказаться от жирной и жареной еды, алкоголя. Если вы активно занимаетесь физическими нагрузками, то до исследования необходимо снизить их количество. Курить разрешено лишь за 40 минут до забора крови.
Перед назначением исследования необходимо обсудить с лечащим врачом препараты, которые вы принимаете регулярно. Возможно, придется на некоторое время приостановить прием лекарственных средств для получения корректного результата.
Норма МНО
Стандартизированная норма МНО — 0,85—1,15 единиц. Если человек принимает антикоагулянты, то его показатель МНО повышен, что закономерно: кровь пациента содержит меньше факторов свертывания. В этом случае норма МНО для пациента составляет 2—3 единицы.
На показатель МНО крови влияет множество факторов, начиная от пола и возраста пациента, заканчивая особенностями его анамнеза. В зависимости от возраста пациентов выделяют следующие границы нормы МНО крови:
Таблица 1. Показатель МНО в зависимости от возраста пациента
| Возраст пациента | Нормальный показатель МНО (в единицах) |
| Период новорожденности, а также первый год жизни | 0,9— 1,25 |
| 1 год— 6 лет | 0,95— 1,1 |
| 12— 16 лет | до 1,35 |
| более 16 лет | 0,85— 1,3 |
Как видно, МНО крови по возрастам — показатель, который существенно меняется в зависимости от категории, в которой относится пациент.
Профилактика
Если лечение галактоземии началось вовремя, исход благоприятный: дети развиваются нормально и чувствуют себя хорошо (если нет погрешностей в диете). Так как болезнь связана с генетическими нарушениями, избавиться от заболевания полностью невозможно. Однако можно значительно облегчить самочувствие и жизнь ребенку, придерживаясь безлактозного питания. Строгая диета обязательна для всех детей, у которых галактоземия диагностирована. Избежать появления признаков катаракты, разрушения клеток печени и задержек в психомоторном развитии можно!
Если диагностику не успели провести вовремя, и произошло поражение органов, с помощью медикаментозной терапии можно значительно замедлить развитие болезни и ухудшение состояния. Если же лечение при галактоземии не проводится вообще, ребенок погибает на протяжении нескольких месяцев.
Чтобы предупредить развитие болезни, нужно учитывать ее наследственные особенности. Для этого будущие родители могут пройти консультацию у генетика (особенно рекомендуется тем, у кого в семье уже рождались дети с галактоземией). За ребенком, у которого диагностирована галактоземия, наблюдает педиатр, диетолог, генетик, невролог.
Чем опасно заболевание?
Избыток галактозы и ее метаболитов приводит к повреждению тканей и органов. Симптомы проявляются у новорожденных в первые дни жизни, поскольку галактоза из грудного молока или молочных смесей попадает в организм и не усваивается должным образом.
Какие метаболиты галактозы токсичны в большом количестве?
При галактоземии в организме больного кроме галактозы может накапливаться галактозо-1-фосфат. Кроме этого, в отсутствии необходимых ферментов метаболизм галактозы протекает иначе: она превращается в галактитол. У больных всегда наблюдается накопление галактитола в крови и тканях и повышение его выделения с мочой.
Какие ткани и органы страдают?
Накопление галактитола в хрусталике глаза обуславливает катаракту — частый симптом галактоземии. Помимо нарушения зрения, у младенцев с галактоземией на фоне грудного вскармливания начинаются такие клинические проявления:
- Симптомы отравления: тошнота, рвота, диарея, вялость;
- Мышечная гипотония;
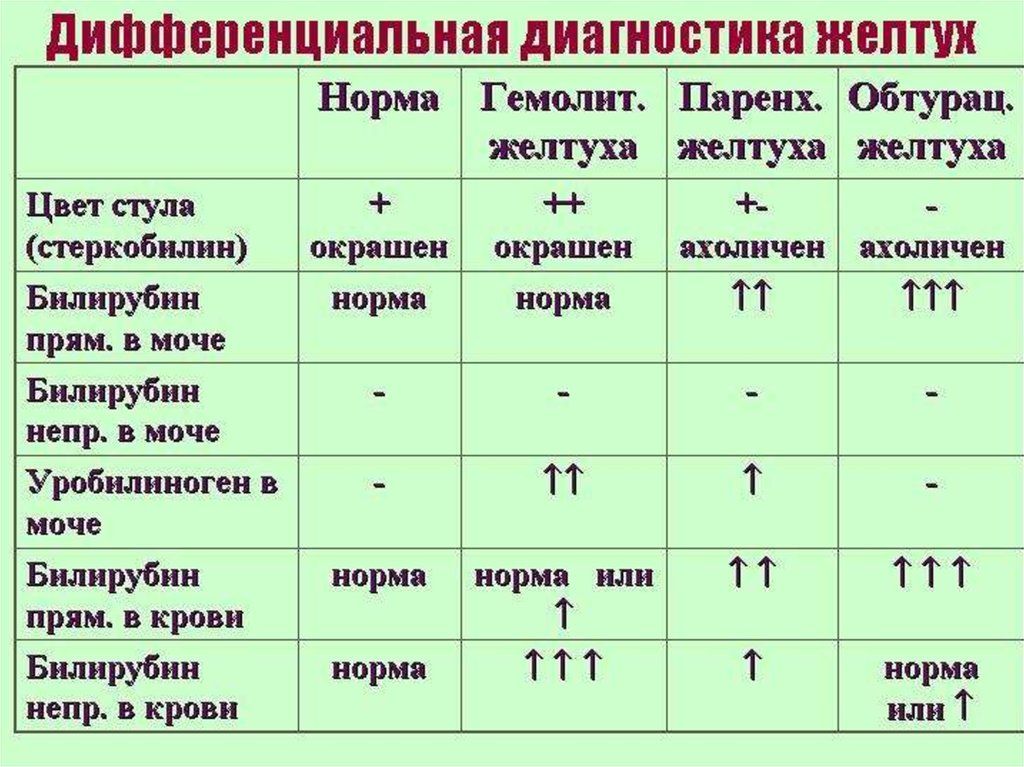
- Нарушается поражение печени, часто сопровождающиеся желтухой и гепатомегалией печени;
- Кровоточивость, связанная с гипокоагуляцией — нарушением свертываемости;
- Нарушение функции почек.
Наиболее тяжелое и обычно фатальное проявление галактоземии — сепсис, в 90% случаев развивающийся из-за кишечной палочки (Escherichia coli).
Что будет, если не лечить галактоземию?
Без своевременной диагностики и лечения около 75% больных умирает во младенчестве: от сепсиса, печеночной недостаточности и других осложнений.
У выживших детей без лечения развивается хроническая печеночная недостаточность и тяжелое поражение нервной системы, которое приводит к задержке психомоторного развития. В итоге такие дети становятся инвалидами, продолжительность их жизни невелика.
Признаки
Ввиду того, что заболевание считается генетическим, его симптоматика определяется исключительно по клинической степени тяжести протекания.
Первоначальная легкая степень проявляется и характеризуется:
- отказом от пищи;
- задержкой речевого развития (вернее, проявления эмоций голосом);
- отставанием в наборе необходимой массы тела (наблюдается анорексия);
- поражением печени токсическими веществами (развиваются хронические заболевания печени);
- поражением центральной нервной системы.
Средняя форма тяжести имеет такие признаки:
- частая рвота;
- развитие желтухи различной степени;
- анемия;
- отставание психомоторного развития;
- развитие катаракты;
- печеночная недостаточность.
Тяжелое протекание галактоземии фиксирует:
- очень раннее развитие (в течение двух дней после появления ребенка на свет);
- появление рвоты у грудничка вскоре после кормления молоком или молочной смесью;
- развитие расстройства стула (появляется водянистый понос);
- нарастание степени интоксикации;
- общую вялость грудничка;
- отказ от еды (грудное молоко или бутылочка);
- отсутствие набора массы тела (развивается выраженная анемия);
- кишечные колики;
- чрезмерный метеоризм;
- обильность отхождения газов;
- стойкая желтуха;
- снижение рефлексов новорожденного;
- развитие печеночной недостаточности;
- цирроз печени;
- увеличение селезенки;
- поражение почек;
- обоесторонняя (на обоих глазах) катаракта;
- замедление в физиологическом развитии.
Кроме того, существует и так называемый асимптомный (безсимптомный) тип галактозесии Дюарте. Он никак не проявляется и может быть обнаружен исключительно по результатам биохимического исследования крови.